סכנה אוטואימונית מהחיסון לקורונה?
תודה גדולה לד״ר רועי מזור ולד״ר אירה זרצקי (אימונולוגיה) וכן לד״ר נעם לויתן (ביולוגיה) על העזרה בהכנת והגהת הפוסט
לאחרונה נפוץ חשש מסכנה אוטואימונית כתוצאה מהחיסון לקורונה והמקור לחשש ככל שראיתי הוא בפוסט שכתבה רופאה בשם מיכל הרן. ד״ר הרן היא המטולוגית ללא התמחות ספציפית בתחום האימונולוגי, וחוסר הידע הרלוונטי ניכר בפוסט, ששותף עד כה באופן ישיר מעל 1,300 פעם (ואין לדעת כמה פעמים נוספות שותף באמצעות העתקה).
על רובם הטעויות בפוסט התעכבה חוות הדעת שפורסמה כאן ושרשימת מחבריה כוללת אימונולוגים ואנשי מקצוע רלוונטיים רבים (ד״ר דיצה לוין – תואר שלישי באימונולוגיה, ד״ר אורן קובילר – רופא MD וכן בעל תואר שלישי במיקרוביולוגיה, ד״ר נטע סופר צור – תואר שלישי באימונולוגיה, ד״ר אירה זרצקי – תואר שלישי באימונולוגיה, ד״ר אורי פלביץ׳ – תואר שלישי בנוירואנדוקריולוגיה, ד״ר דודי שטיינר – תואר שלישי באימונולוגיה, ד״ר נעם לויתן -תואר שלישי בביולוגיה מולקולרית, ד״ר דרור בר ניר – תואר שלישי בביולוגיה מולקולרית, ד״ר רועי מזור – רופא MD ודוקטורנט באימונולוגיה, ענר אוטולנגי – דוקטורנט באימונולוגיה, ד״ר מורן פרידמן – רופאה MD מומחית לרפואה פנימית, רופאים וחוקרים נוספים).
עם זאת, על הנקודה האוטואימונית אפשר להרחיב מעט יותר.
ראשית, הקטע הרלוונטי מהפוסט:
“השיטה שפותחה גורמת לתאי השריר לייצר חלבון ששייך לוירוס ולהציג אותו על מעטפת התא. כלומר זה הופך את תאי השריר לתאים זרים, באופן זמני, רק עד שתאי מערכת החיסון יבינו שהם צריכים לייצר נגדם נוגדנים.
הבעייה שלא ברור לי איך אנחנו נסביר לתאים של המערכת החיסונית שהתא הזר שהם צריכים לתקוף הוא לא באמת תא זר, אלא תא שריר רגיל ובריא ושהם צריכים לייצר נוגדנים רק נגד החלבון של הנגיף ולא נגד חלבונים אחרים שנמצאים לידו.
זה לא רק חשש תיאורטי, אלא תופעה מוכרת מהתחום שנקרא cancer immunotherapy. אחת הסכנות אצל חולים עם סרטן מתקדם שמקבלים תרופות שנועדו להפעיל את מערכת החיסון נגד תאי הסרטן היא התפתחות של נוגדנים עצמיים עד כדי מחלות אוטואימוניות קשות ומסוכנות.
יש לכך דוגמא מצערת מתחום המומחיות שלי. טיפול גנטי שנועד לגרום לתאים של מח העצם לייצר חלבון שחסר במחלה בשם SCID גרם אצל חלק מהילדים שקיבלו אותו לסרטן דם קשה אחרי 3-6 שנים”
מראש לא הייתי ממליץ (בלשון המעטה) לגבש דעה לפי דעת מיעוט של מישהי שאינה מצויה בתחום, ובאותו הזמן להתעלם מדעתם של רוב מוחלט מהאימונולוגים בארץ ובעולם שזהו תחום מומחיותם (כולל אנשי המקצוע מהשורה הראשונה שישבו בוועדת ה-FDA שאישרה את החיסון, בדיון שבוצע בשקיפות מלאה ושודר לעיונם של כל האימונולוגים בעולם). אם בכל זאת מחליטים להיות ״חוקר עצמאי״ צריך להבין קצת יותר איך הדברים עובדים ולא להתמסר להפחדות על בסיס חוסר הבנה.
כפי שקובע חוק ברנדוליני – ״המאמץ הנדרש כדי להפריך בולשיט גדול לפחות פי עשרה מזה שנדרש כדי ליצור אותו״. קל הרבה יותר להפחיד ולזרוק משהו ש״נשמע נכון״ מאשר להבין באמת איך הדברים פועלים. כדי להגיע לשורש הדברים צריך להבין לפחות מושגי יסוד, אבל אנסה להזדקק לכמה שפחות מונחים טכניים.
מה קורה בתא אליו חודר נגיף או חיסון
כאשר נגיף הקורונה מדביק תא בגופנו, הנגיף משעבד את מנגנוני הייצור של התא אליו פלש, ומשתמש בהם לייצר עוד עותקים של עצמו. רוב העותקים יוצאים מהתא כשהם שלמים, בתהליך הנקרא אקסוציטוזיס (Exocytosis) שניתן לראות באיור להלן.
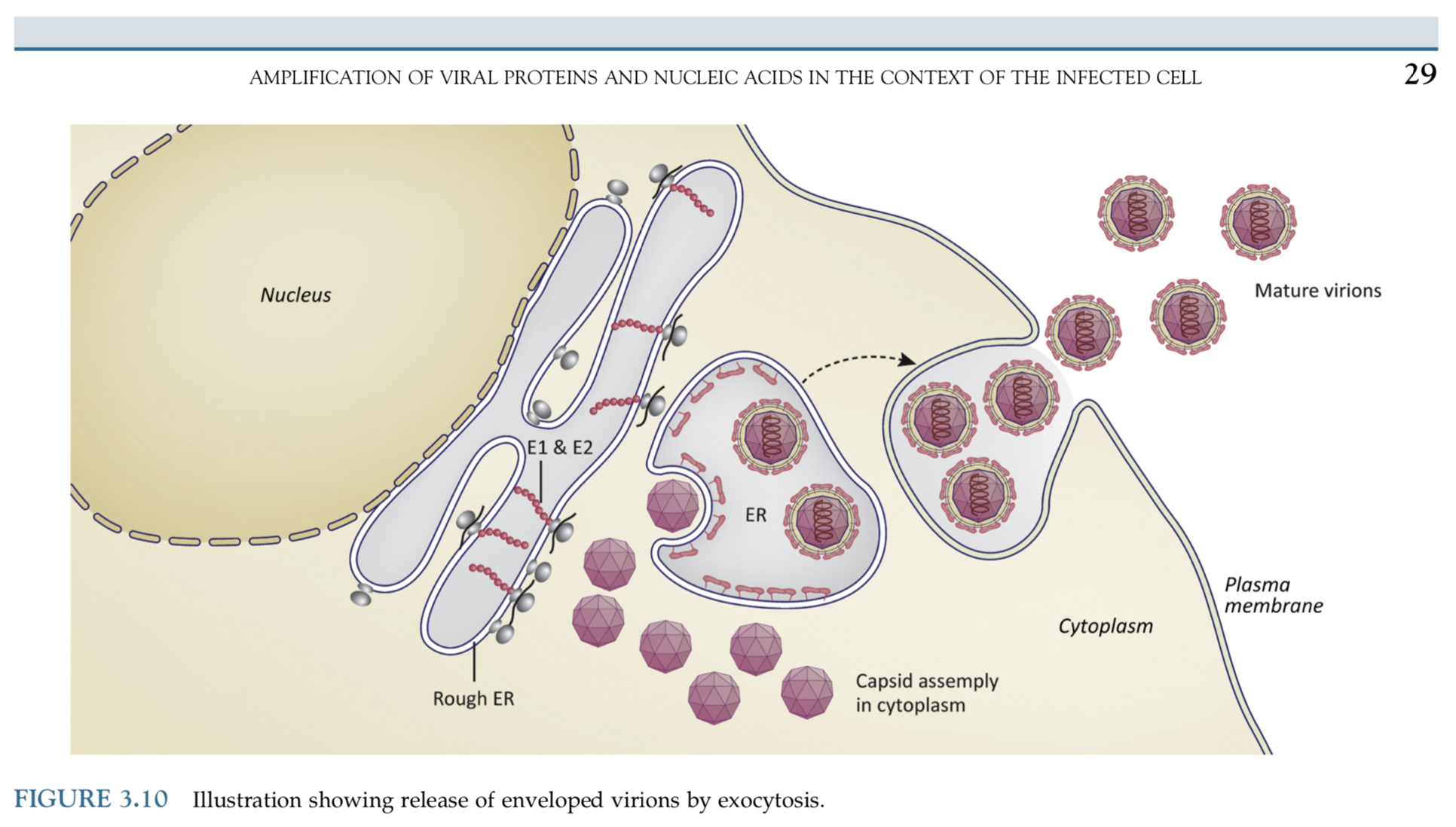
אקסוציטוזיס של ויריונים | מקור: Viruses (פרק 3)
תאים הנגועים בנגיף ישתמשו במולקולה מיוחדת בשם MHC1 כדי להציג על הקרום החיצוני שלהם רצפים חלבוניים קצרים הקרויים פפטידים, שמקורם בחלבונים של הנגיף הפולש. זהו למעשה איתות למערכת החיסון להיכנס לפעולה ולהשמיד את התא הנגוע באמצעות תאי הרג מיוחדים (תאי T ציטוטוקסיים). התאים הללו מושמדים ואינם באים במגע באף נקודה עם מערכת החיסון הנרכשת.
במקביל, חלק מהחלבונים הזרים נאספים על ידי תאי שליח מיוחדים (מאקרופאג׳ים, תאי B ותאים דנדריטיים), שתפקידם לזהות חלבונים שאינם אנושיים, לאסוף אותם ולהציג אותם לתאי עזר (Helper T cells) ששייכים למערכת החיסונית הנרכשת. תאי העזר הללו הם אלה המשמשים ללימוד והכנת ההגנות ייעודיות נגד הפולש ואחסון הזיכרון אודותיו לזיהוי עתידי. התאים השליחים מציגים להם את החלבונים שאספו באמצעות מולקולה אחרת, הנקראת MHC2, איתה הם מציגים על הקרום החיצוני שלהם את החלבונים הזרים.
אחסון הזיכרון החיסוני על החלבון הזר, אם כן, כלל לא מתבצע על גבי תאי השריר הנגועים, שכן אלו מושמדים באמצעות תאי ההרג בגלל שזה מה שקורה לתא המציג על גבי MHC1. תאי השליח המיוחדים מציגים את החלבון הזר וחלקיו על גבי MHC2, ולכן הם אלו שיכולים לתקשר עם המערכת החיסונית הנרכשת. אין אפשרות, ברמה המולקולרית, ״להתבלבל״ בין MHC1 ל-MHC2.
נסכם:
הטענה הבסיסית כאן לגבי החיסון לקורונה היא שכאשר מוצג חלבון זר על גבי קרום התא (במקרה הזה – תא שריר), מערכת החיסון עלולה להתבלבל ולאחסן זיכרון שגוי לפיו עליה לתקוף את סוג התאים הזה. אלא שלמנגנון הביולוגי הבסיסי בגוף שבאמצעותו מאוחסן זיכרון חיסוני אין כל קשר לתאי השריר.
יש כן אפשרות נדירה שאפשר להעלות על הדעת – עליה בחלק הבא.
הצגת חלבונים זרים – ההבדל בין מחלה לחיסון
תאי העזר של המערכת החיסונית הנרכשת לא פוגשים אם כן את תאי השריר, ולא מאחסנים זיכרון עבורם גם אם יציגו חלבונים זרים על הקרום שלהם. אבל מה לגבי המאורע הנדיר בו מתרכב חלבון זר עם חלבון מהתא? תהליך זה עשוי לקרות, גם אם בהסתברות נמוכה מאד, תאי השליח עשויים לקחת את הקומפלקס שנוצר לתאי העזר של המערכת החיסונית הנרכשת ועלולה להיווצר בעיה. נבחן את ההיגיון שזה יקרה בחיסון, בהתחשב בכך שאצל חולי קורונה זה קורה באופן נדיר ורק במקרים של תחלואה קשה מאד.
כפי שראינו, גם במקרה של חיסון וגם במקרה של הידבקות בנגיף ישתמשו התאים שנפלשו ב-MHC1 כדי להציג על הקרום שלהם חלקי חלבונים מנגיף הקורונה. ההבדל העיקרי הוא שבמקרה של הידבקות בנגיף הרבה יותר תאים צפויים להיפלש, כיוון שהנגיף משתכפל באופן מעריכי (טור הנדסי), זאת לעומת החיסון שמולקולת ה-mRNA שבו חודרת לתא אליו בלבד, אינה משתכפלת, מייצרת את החלבונים הנגיפיים שתוכננה לייצר ואז מתפרקת. כאמור מקרה של יצירת קומפלקס (חיבור קוולנטי בין חלבון זר לחלבון עצמי) הינו נדיר וקורה רק כשהעומס הויראלי עצום (מקרים של תחלואה קשה מאד), מצב בו יש סדרי גודל רבים של תאים נגועים יותר מאשר במקרה של החיסון.
במקרה של הידבקות בקורונה תהיה אם כן הצגה של מספר חלבונים על קרומיהם של הרבה יותר תאים מאשר במקרה של חיסון. בנוסף, במקרה של הידבקות התא נפלש על ידי הוירוס כולו, ולכן יוצג מגוון גדול יותר של חלבוני נגיף. לעומת זאת החיסון מכיל חלבון אחד בלבד מהנגיף (חלבון הספייק), והוא היחיד שחלקיו יוצגו.
לא זו בלבד, אלא שבמקרה של תחלואה בקורונה התאים הנגועים יהיו בעיקר בדרכי הנשימה, ולעומת זאת בחיסון מדובר על תאי שריר, שיש בהם פחות מחצי מכמות ה-MHC1 שיש בתי ריאה (רצ״ב גרף). כלומר, לא רק שבמקרה של מחלה יהיו הרבה יותר תאים נגועים מאשר בחיסון, אלא שגם כל תא נגוע אופייני יציג יותר מפי שתים חלבונים מאשר יוצגו על ידי תא המופעל על ידי החיסון.
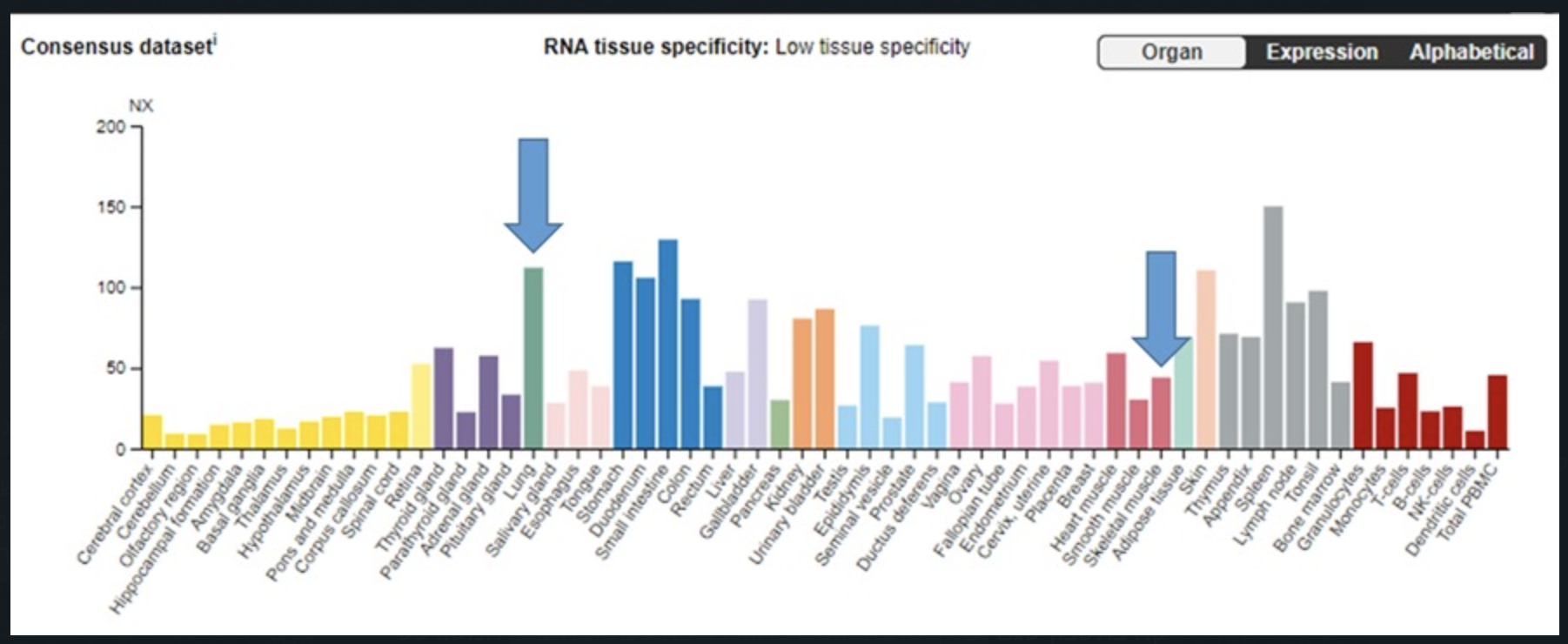
כמות ה-MHC1 ברקמות אנושיות שונות | מקור: BMC Medical Genomics
נסכם:
השאלה הייתה מה הסבירות להניח מקרה של התרכבות חלבונית היוצרת בעיה כתוצאה מהחיסון לעומת כתוצאה מהידבקות בקורונה? התשובה היא לא רק ״הרבה פחות סביר״ אלא ״הרבה פחות סביר בחזקת 3״, כי:
- קורונה גורמת להצגה של יותר סוגי חלבונים זרים על כל תא מאשר חיסון לקורונה,
- קורונה גורמת להרבה יותר תאים להציג חלבון זר מאשר חיסון לקורונה, בוודאי קורונה קשה (שלמיטב ידיעתי רק בה נתגלה, ולעיתים נדירות, מצב כזה),
- בקורונה כל תא מציג יותר מכפליים חלבון זר מאשר בחיסון לקורונה.
בקיצור, בהתחשב בכך שבעיות אוטואימוניות הן נדירות בעקבות תחלואה בקורונה ורק בעקבות מקרים קשים, הסיכוי לצפות להן כתוצאה מחיסון אמנם אינו אפס, אבל קרוב מאד לכך.
עד כמה עלולים חלבוני הקורונה לבלבל את המערכת החיסונית
– אמנם ראינו שהסבירות אפסית שהחיסון יגרום לאוטואימוניות נגד תאי שריר,
– ואמנם ראינו שכל טענה נגד החיסון על בסיס ״הצגת חלבון זר״ צריכה להיטען בסדרי גודל יותר נגד המחלה עצמה,
– אך מעבר לכך, מהי האפשרות לחקיינות מולקולרית (Molecular Mimicry) של נגיף הקורונה את החלבונים האנושיים? אחרי הכל, כדי שמערכת החיסון ״תתבלבל״ בין חלבונים, נדרש דמיון מסויים ביניהם.
״הוראות הייצור״ לנגיף הקורונה, לאדם ולמעשה לכל היצורים החיים כתובות באמצעות קוד גנטי, שפה המאוייתת באמצעות מולקולות מיוחדות המכונות ״נוקלאוטידים״. האם רצף הנוקלאוטידים של חלבון הספייק, זה שההוראות לייצורו מצויות בחיסון, דומה לרצף של חלבון כלשהו של בני אדם ועלול לכן ליצור בלבול? כדי לבצע השוואות מסוג זה נבנו אלגוריתם ותוכנה מיוחדים בשם Protein BLAST. במאגר המידע של התוכנה יש את כל רצף הפרוטאום האנושי, וניתן לבקש השוואה בינו לבין כל רצף מוגדר, לפי קריטריונים כמבוקש.
ובכן, בהרצה של רצף הספייק מהחיסון תחת ההנחיה להראות כל חלבון שנותן דמיון (הומולוגיה) של 5% ומעלה לחלבון אנושי כלשהו מקבלים פשוט אפס תוצאות. אין ולו חלבון אנושי אחד שדומה אפילו עד כדי 5% לחלבון הספייק. גם אם נחפש דמיון בין שברים של הספייק לחלבונים אנושיים, ונפרק את הרצף מהחיסון ל-51 פפטידים קצרים של 24-25 חומצות אמינו (אבני הבניין שלהם), וגם אם ננמיך את מידת הדמיון הנדרש להתאמה חלקית של עד 30%, עדיין לא מוצאים התאמה אפילו לא לחלבון אחד של בני אדם.
מסתבר שהקורונה רחוקה מאיתנו כל כך מבחינה אבולוציונית שאין אפילו קרבה מינימלית, ובוודאי שלא במידה שמספיקה לבצע הסטה של התגובה החיסונית לתגובה אוטואימונית. אין כל בסיס הגיוני לפיו נוכל לצפות לחקיינות מולקולרית.
קשר לאימונותרפיה בסרטן?
הפוסט מביא אימונותרפיה בסרטן כדוגמה לסיטואציה בה נוצרות תופעות אוטואימוניות. אלא שבניגוד לנגיף הקורונה, התאים הסרטניים הם אנושיים ודומים מאד לתאים הרגילים. זו הסיבה שלצורך הטיפול האימונותרפי מבצעים החלשה מכוונת של הבלמים במערכת החיסון, במטרה לאפשר תקיפה עצמית של מערכת החיסון את תאי הגוף, ובעיקר הסרטניים שבהם כמובן, מתוך ידיעה שזה המחיר הנדרש כדי לעזור למטופל.
באדם שאינו עובר אימונותרפיה עוברים תאי ה-T של מערכת החיסון אימון (בבלוטת התימוס) במסגרתו הם נבדקים מול כל הפנורמה של החלבונים האנושיים. תאים שמראים תוקפנות כלפי חלבונים עצמיים מושמדים עוד שם, בבלוטת התימוס. למרבה הצער, החלבונים של תאים סרטניים לא מובדלים מספיק מהחלבונים העצמיים, כי מקורם בתא רגיל (שעבר מוטציה), ותאי ה-T לא יתקפו אותם אם לא ״נקלקל״ את האימון שהם עוברים. מהות הטיפול האימונותרפי אם כן היא יצירת מצב אוטואימוני, בו פוגעים בכוונה בבלמים ובאיזונים של תאי ה-T כדי שהם יוכלו לאתר ולחסל תאים אנושיים, עם חלבונים אנושיים.
כאשר עושים זאת אין ספק שמשחקים משחק מסוכן כי פגיעה באותם איזונים ובלמים תגרור גם תקיפה של תאים בריאים. מצב אוטואימוני שעלול למשל לגרום לפגיעה בעור, בעיניים ובשיער (מלנוציטים בריאים) בדרך לחיסול תאי מלנומה חולים. אבל האיזון המסוכן הזה משתלם כדי לעזור למטופל: רק לפני מספר שנים הישרדות ל-5 שנים במלנומה עמדה על 5%, ואילו היום כבר יש טיפולים אימונותרפיים שככל הידוע מרפאים לחלוטין אחוז מסויים של מלנומה אפילו כשהמחלה מפושטת עם גרורות למוח.
אז כן, באימונותרפיה בסרטן פוגעים במערכת החיסונית, במתכוון, ויוצרים מצב אוטואימוני מבוקר. אבל מה הקשר בין זה לבין החיסון לקורונה? חלבוני הקורונה השונים באופן קיצוני מהחלבונים האנושיים. הספייק של הקורונה המיוצר בחיסון שונה כל כך מחלבונים האנושיים שאין כל צורך להחליש את מנגנוני ההגנה של המערכת החיסונית, וממילא לא יוצרים מצב אוטואימוני. זה פשוט לא קשור, לא נכון ולא קורה.
טיפול גנטי ל-SCID
הפוסט מסתיים בסיפור עגום אודות ״טיפול גנטי במחלה בשם SCID, שגרם אצל חלק מהילדים שקיבלו אותו לסרטן דם קשה אחרי 3-6 שנים״. אכן רע מאד, וכפי שאכן קורה לעיתים בניסיון הנואש לפתח טיפולים ניסיוניים למחלות סופניות דוגמת SCID, שילדים הנולדים איתה צפויים למות בטרם תמלא להם שנה אחת אם לא יטופלו.
אלא שכפי שכותבת ד״ר הרן, אכן מדובר בטיפול גנטי, כלומר באמצעות שינוי ה-DNA שבגרעין התאים של המטופלים. חשוב להבין שה-DNA הוא מולקולה יציבה להפליא, ששורדת בשלמותה לאורך כל חיי האדם מרגע הפריית הביצית ממנה יווצר ועד יום מותו. מטרתו של טיפול גנטי היא להישאר בגוף זמן רב ככל האפשר, ולכן בוצעה כניסה לגרעין ויצירת שינוי ב-DNA. יש לציין גם שחיי כל המטופלים הוארכו בעקבות הטיפול במספר שנים ביחס למצבם המשוער ללא טיפול, גם אם אכן נותרה עוד עבודה רבה לשיפור התרפיה הגנטית האמורה.
החיסון, לעומת זאת, מתבצע באמצעות מולקולה אחרת ששמה mRNA ושהינה שבירה ביותר. מכאן גם הצורך לאחסן את החיסונים בטמפרטורות מתחת לאפס, שכן אחרת ה-mRNA יתחיל להתפרק תוך שעות.
בחיסון נכנסות לגוף מולקולות ה-mRNA כאשר הן עטופות בבועות שומניות זעירות ששומרות עליהן (Lipid Nano Particle או LNP). כאשר ה-mRNA פוגש בכל תא בו הוא אמור לבצע את עבודתו, הוא משתחרר מהבועה השומנית המגנה עליו והספירה לאחור לקראת סוף חייו מואצת. המולקולה נשארת בנוזל התא (הציטופלזמה) למשך כמה שעות, שם רכיב בתא (ריבוזום) מתרגם את המידע שבה ליצירת חלבון של נגיף הקורונה (הספייק) כדי שמערכת החיסון תוכל ללמוד אותו. עם תום התהליך, ובתוך כמה שעות מרגע כניסתה לתא, מולקולת ה-mRNA מתפרקת לאבני הבניין המרכיבות אותה (נוקלאוטידים), שמופרשים מהגוף או ממוחזרים.
הבלבול בין טיפול גנטי המשנה את ה-DNA לבין חיסון mRNA עשוי להישמע קביל למי שאינו מצוי בתחום אך משול לבלבול בין בועת סבון לכדור ברזל, טעות שאם היינו שומעים ממישהו שמתיימר להבין באתלטיקה, סביר שלא היינו טורחים להמשיך להאזין ליתר עצותיו המלומדות.
סיכום
הפוסט טען לבעיה אוטואימונית בשרירים, בהתבסס לכאורה על הצגת חלבון זר על תאי שריר כתוצאה מהחיסון. קשה לראות איך יש לטענה זו משקל:
- ככל שרואים, אין דמיון בין חלבון הספייק של הקורונה לבין חלבונים אנושיים,
- החיסון גורם להצגה של הרבה פחות חלבון זר מאשר כשנדבקים בקורונה,
- וממילא החלבון הזר המוצג על תאי השריר אינו קשור לזכרון החיסוני שנשמר אודות הפולש, אלא במקרים של יצירת קומפלקס שאפילו במקרים של מחלה קשה הם נדירים כך שההסתברות לקבלם מחיסון לפי הערכת אנשי המקצוע נמוכה ביותר.
תוספות לא קשורות שמספרות על טיפולים אימונותרפיים או גנטיים נוספו לצרכי הפחדה בלבד. באותה מידה אפשר היה לקשט את הפוסט בתמונה של כריש או של ליצן מפחיד. זה גם היה קשור באותה המידה.

אימונותרפיה! הנדסה גנטית! איידס! דבורים קטלניות! חיסון קורונה!
במבחן המציאות, חוסנו מעל 35,000 איש בניסויים של פייזר ומודרנה ועברו כבר מספר חודשים בלי שנמצא מקרה של נוגדנים אוטואימוניים נגד תאי שריר. בחודש האחרון חוסנו עוד מיליונים – כנ״ל.
אם היה מצב כזה הרי שלפי הידע שנאסף עד היום היתה ציפיה לכאבי שרירים, חולשה שרירית, פגיעה ברקמות וכו’ בתוך שבועיים-שלושה (זאת בהתבסס על מקרים של תופעות אוטואימוניות אחרי תחלואה ויראלית כגון מחלות לב ראומטיות אחרי דלקת סטרפטוקוקלית, ITP וכו׳).
האם ניתן לקבוע שהסיכון מהחיסון הוא אפס? לא. לקבל החלטה בעולם האמיתי משמעותה בהכרח פעולה בתנאי אי וודאות וביצוע הערכת סיכונים. כל פרוצדורה רפואית יש סיכון בצידה. גם לחיסון ותיק כמו לחצבת יש תופעות לוואי קשות במקרים נדירים ואם נופלים בלוטו הזה זה איום ונורא. אבל לעומת זאת הסיכון שבאי-התחסנות גדול לאין שיעור. השאלה אינה ״האם אפשר להיות בטוחים ב-100% שאין סיכון״ כי זו ברירה כוזבת.
בחירה היא תמיד מבין האופציות הקיימות, לא מבין הרצויות. הבסיס לקבלת החלטה רציונלית הוא הידע המקצועי שנצבר, ובהתבסס על הידע שנאסף עד היום יש קונצנזוס מקצוע גורף בין אנשי המקצוע הרלוונטיים שהסיכון המשוער בחיסון נמוך בסדרי גודל מהסיכון המשוער מהמחלה.
מאז התפרצות הקורונה בישראל חלו קשה מעל 15,000 איש ומתוכם מתו מעל 3,500. אולי בכל זאת נקשיב לאנשים שלמדו את הנושא כל חייהם ויודעים על מה הם מדברים, במקום לאנשים שאין להם הכשרה רלוונטית?